Bảng kí hiệu Hóa học lớp 8 là tài liệu vô cùng hữu ích mà Download.vn muốn giới thiệu đến quý thầy cô cùng các bạn học sinh tham khảo.
Đang xem: Bảng hóa trị lớp 8 của một số nguyên tố hóa học thường gặp
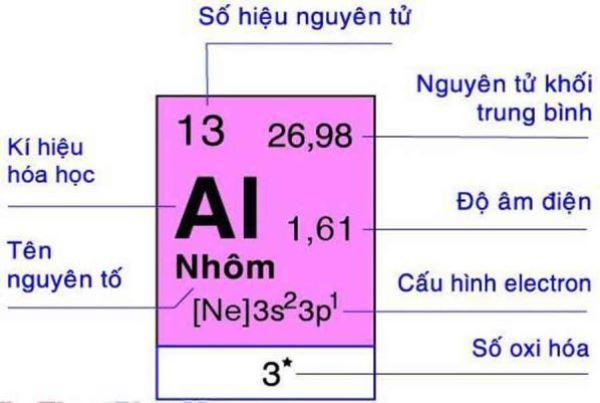
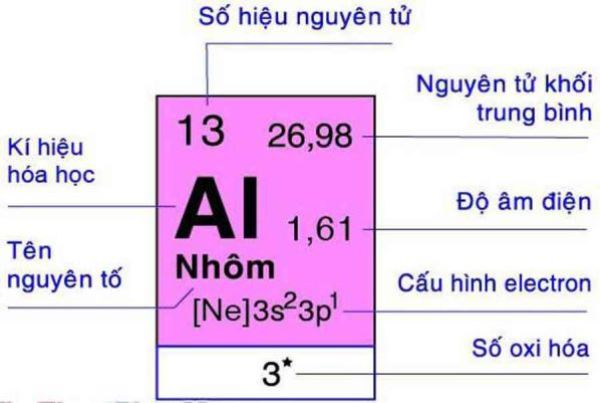
Trong hóa học, các kí hiệu trong Hóa học 8 là tên viết tắt của một nguyên tố hóa học. Biểu tượng cho các nguyên tố hóa học thường bao gồm một hoặc hai chữ cái trong bảng chữ cái Latinh và được viết với chữ cái đầu tiên viết hoa. Vậy sau đây là nội dung chi tiết tài liệu, mời các bạn cùng theo dõi tại đây.
Xem thêm: Bán Thùng Loa Đóng Thùng Loa Ở Tại Tphcm, Nhận Đóng Loa Thùng Theo Yêu Cầu
Các kí hiệu trong Hóa học 8
A. Bảng kí hiệu hóa học lớp 8 trang 42
| Số proton | Tên Nguyên tố | Ký hiệu hoá học | Nguyên tử khối | Hoá trị |
| 1 | Hiđro | H | 1 | I |
| 2 | Heli | He | 4 | |
| 3 | Liti | Li | 7 | I |
| 4 | Beri | Be | 9 | II |
| 5 | Bo | B | 11 | III |
| 6 | Cacbon | C | 12 | IV, II |
| 7 | Nitơ | N | 14 | II, III, IV… |
| 8 | Oxi | O | 16 | II |
| 9 | Flo | F | 19 | I |
| 10 | Neon | Ne | 20 | |
| 11 | Natri | Na | 23 | I |
| 12 | Magie | Mg | 24 | II |
| 13 | Nhôm | Al | 27 | III |
| 14 | Silic | Si | 28 | IV |
| 15 | Photpho | P | 31 | III, V |
| 16 | Lưu huỳnh | S | 32 | II, IV, VI |
| 17 | Clo | Cl | 35,5 | I,… |
| 18 | Argon | Ar | 39,9 | |
| 19 | Kali | K | 39 | I |
| 20 | Canxi | Ca | 40 | II |
| 24 | Crom | Cr | 52 | II, III |
| 25 | Mangan | Mn | 55 | II, IV, VII… |
| 26 | Sắt | Fe | 56 | II, III |
| 29 | Đồng | Cu | 64 | I, II |
| 30 | Kẽm | Zn | 65 | II |
| 35 | Brom | Br | 80 | I… |
| 47 | Bạc | Ag | 108 | I |
| 56 | Bari | Ba | 137 | II |
| 80 | Thuỷ ngân | Hg | 201 | I, II |
| 82 | Chì | Pb | 207 | II, IV |
Chú thích:
Nguyên tố phi kim: chữ màu xanh
Nguyên tố kim loại: chữ màu đen
Nguyên tố khí hiếm: chữ màu đỏ
HOÁ TRỊ CỦA MỘT SỐ NHÓM NGUYÊN TỬ
| Tên nhóm | Hoá trị | Gốc axit | Axit tương ứng | Tính axit |
| Hiđroxit(*) (OH); Nitrat (NO3); Clorua (Cl) | I | NO3 | HNO3 | Mạnh |
| Sunfat (SO4); Cacbonat (CO3) | II | SO4 | H2SO4 | Mạnh |
| Photphat (PO4) | III | Cl | HCl | Mạnh |
| (*): Tên này dùng trong các hợp chất với kim loại.
Xem thêm: Top 14+ Kem Béo Thực Vật Rich'S Creamer, Kem Béo Thực Vật Rich'S Creamer |
PO4 | H3PO4 | Trung bình | |
| CO3 | H2CO3 | Rất yếu (không tồn tại) |
B. Kí hiệu các công thức hóa 8
I. Cách tính nguyên tử khối
NTK của A = Khối lượng của nguyên tử A tính bằng gam : khối lượng của 1 đv
C tính ra gam
Ký hiệu hoá học là nội dung vô cùng quan trọng khi các em làm quen với bộ môn Hoá. Những ký hiệu này xuất hiện trong suốt quá trình học lý thuyết, làm bài tập và bài kiểm tra. Vậy bảng ký hiệu hóa học là gì? Cách đọc chúng trong bảng tuần hoàn hóa học như thế nào? Các em hãy cùng chúng tôi tìm hiểu ngay qua bài viết sau.


Những Món Đồ Cực Kỳ Cần Thiết Cho Mẹ và Bé Yêu Đang MIỄN PHÍ Vận Chuyển và Giảm Tới 50% |
|||
|
|
|
|
|
| Khăn Che Bé Bú Đa Năng
Mua Ngay |
Yếm Ăn Dặm Chống Thấm
Mua Ngay |
Mũ Len Lót Lông Cừu
Mua Ngay |
Dép Tập Đi Chống Ngã
Mua Ngay |
Những Món Đồ Cực Kỳ Cần Thiết Cho Mẹ và Bé Yêu Đang MIỄN PHÍ Vận Chuyển và Giảm Tới 50% |
|||
|
|
|
|
|
| Gối Chống méo Đầu
Mua Ngay |
Khăn Sữa Cho Bé
Mua Ngay |
Khăn Len Ống Cho Bé
Mua Ngay |
Gối Bảo Vệ Lưng Đầu
Mua Ngay |
Những Món Đồ Cực Kỳ Cần Thiết Cho Mẹ và Bé Yêu Đang MIỄN PHÍ Vận Chuyển và Giảm Tới 50% |
|||
|
|
|||
| Áo Choàng Cho Bé Lông Cừu
|








